
抗体人源化改造
在抗体药物开发中,降低免疫原性并保留靶向能力是临床转化的核心挑战。溪长生物凭借CDR移植抗体人源化技术,为全球客户提供科学的解决方案,助力抗体药物安全性与疗效双重突破!
溪长生物——CDR移植抗体人源化技术领航者
在抗体药物开发中,降低免疫原性并保留靶向能力是临床转化的核心挑战。溪长生物凭借CDR移植抗体人源化技术,为全球客户提供科学的解决方案,助力抗体药物安全性与疗效双重突破!
技术优势
准确设计:通过将鼠源/兔源抗体的互补决定区(CDR)准确移植至人源抗体框架区(FR),较大程度保留原始抗体的高亲和力与特异性,同时清理除去异源性风险。
智能优化:基于结构生物学与AI算法,对FR关键残基进行理性设计,增强抗体稳定性与可开发性,避免传统人源化导致的活性损失。
效率验证:结合表面等离子共振(SPR)、免疫原性预测软件及体外/体内功能实验,多方面评估人源化抗体的结合活性与临床安全性。
服务亮点
全周期覆盖:从序列分析、CDR移植、亲和力恢复,到稳定细胞株构建,提供一站式人源化开发服务。
高成功率:依托超50例成功案例经验,人源化抗体免疫原性降低>90%,亲和力保留率>85%。
灵活适配:支持单抗、双抗、scFv及纳米抗体等多种形式,适配肿瘤、自免、感染性疾病等多元领域。
具体内容
通过CDR移植的方法进行小鼠或者其他种属来源的抗体的人源化改造。
以小鼠为例,该方法主要包括以下几个主要步骤:
鼠抗序列分析及CDR区序列 确认:对鼠抗序列进行整体分析,确定CDR区,预测潜在翻译后修饰位点。
人框架区选择:根据同源性比对结果,确认较合适的人源框架区。
回复突变位点:根据抗体轻重链结合以及对CDR loop的影响确认回复突变位点。
基因合成及真核表达质粒构建:将人源化后的抗体氨基酸序列反向翻译成碱基,并进行密码子优化,然后构建至真核表达质粒中。
表达和纯化:瞬转至CHO或者HEK293中进行表达并纯化。
亲和力测定:通过Biacore评估移植后的人源化抗体的亲和力。
CDR移植方法的优势在于保持了原始小鼠源抗体的抗原结合能力,同时减少了小鼠抗体的免疫原性和潜在的不良反应。
服务流程
服务项目 | 具体内容 | 时间 | 结果 |
抗体的人源化设计 | 鼠抗序列分析 人germline的比对与选择 CDR grafting 序列优化 确定回复突变位点 | 2-3天 | 多条人源化序列 |
人源化抗体的重组表达 | 密码子优化及基因合成 真核表达质粒构建 瞬转表达 纯化及QC | 2周 | 纯化的人源化抗体 |
人源化抗体的活性鉴定 | 抗原结合活性及亲和力检测 | 1周 | 确定的人源化序列及报告 |
服务案例
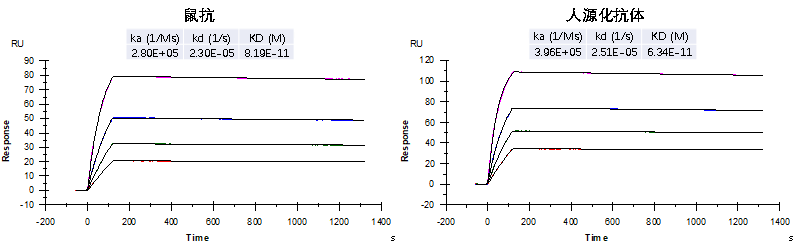
无论是早期抗体人源化改造,还是临床前候选分子优化,溪长生物以创新技术与丰富经验为基石,赋能抗体药物从实验室到市场的全程飞跃。立即咨询,开启低免疫原性、高疗效的抗体开发新篇章!
文件资料


